您现在的位置: 炸金花在线玩» 炸金花在线玩 动态» 【科研新进展】羊遗传改良与生物育种团队在小型化CRISPR工具开发方面取得新突破
【科研新进展】羊遗传改良与生物育种团队在小型化CRISPR工具开发方面取得新突破
作者:栗华 发布日期:2025-10-29 浏览次数:
基因编辑技术被誉为生命科学的革命性突破,它为人类提供了一种直接改写基因密码的能力,使研究者能够精确探索生命奥秘,并在遗传病治疗、动植物育种和合成生物学等领域展现出前所未有的潜能。然而,理想与现实之间依旧存在鸿沟:目前最常用的Cas9和Cas12a虽然功能强大,却因体积庞大而无法顺利装入最安全的体内递送工具AAV载体中,这直接限制了它们在实际应用场景中的发挥。与此同时,现有的碱基编辑器依赖于非靶向链作为反应底物,另一条与sgRNA配对的靶向链则始终无法被编辑,导致大量位于靶向链上的关键突变无法被覆盖。递送受限与编辑范围受限,成为阻碍碱基编辑发挥其全部潜能的“双重枷锁”。正是这种迫切的挑战,驱动科学家们不断探索新的可能——一种既小巧、便于递送,又能突破传统编辑边界的新一代工具。
近日,我校羊遗传改良与生物育种创新团队联合南京大学、南京师范大学等单位,在小体积的Un1Cas12f1基因编辑系统基础上,开发出性能显著提升的变体,并首次开发出能够在DNA的靶向链上实现胞嘧啶脱氨的新型碱基编辑工具。该成果发表于国际期刊《Nature Communications》。
1. 从局限到需求:迷你碱基编辑工具的开发
在现有的基因编辑工具中,Cas9和Cas12a使用最广泛,但它们的体积都超过4 kb,这意味着它们难以被常用的AAV载体装入,而AAV是目前最成熟、最安全的体内递送方式之一。无法递送,就难以走向实际应用。另一个限制来自碱基编辑器本身的工作原理。现有的碱基编辑工具都依赖sgRNA与DNA结合后产生的单链DNA(非靶向链)进行编辑,另一侧与sgRNA配对的靶向链则不能作为编辑对象。这使得许多位于靶向链上的致病突变无法覆盖。因此,一个既小巧易递送,又能拓展编辑范围的工具,成为亟需攻克的方向。
2. 从Un1Cas12f1出发:小巧而高效
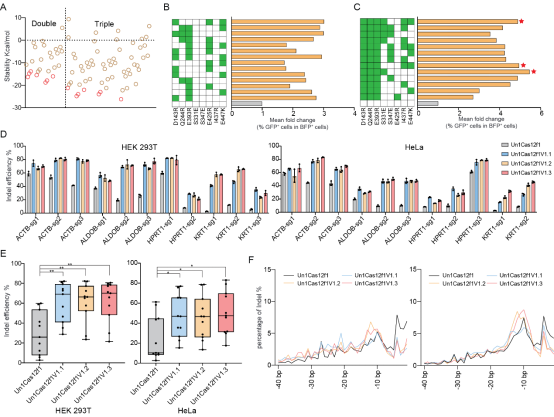
Un1Cas12f1是Cas12家族中最早发现的以二聚体形式发挥功能的Cas蛋白,因为体积小,天然适合AAV载体。但Un1Cas12f1的编辑效率远低于最为常用的Cas9工具。如何在保持“小”的同时,实现“强”,成为关键。联合团队采用了结合计算机建模和突变筛选的策略,他们使用Discovery Studio软件对自由能变化进行预测,寻找可能提升蛋白稳定性的氨基酸位点,再通过饱和突变实验逐一进行验证。经过多轮优化筛选后,最终获得了高性能的编辑工具变体——enUn1Cas12f1。
研究表明,改造后的 enUn1Cas12f1 在多种人类细胞中展现出显著提升的编辑活性,其效率已经接近甚至部分情况下可媲美经典的SpCas9。同时,得益于其紧凑的体积(1587 bp),enUn1Cas12f1可以被完整装入AAV载体,实现单载体高滴度包装,有效解决了AAV递送受限的问题。在动物体内验证中,联合团队将该系统递送至小鼠肝脏,成功实现目标基因的高效敲除(60%),并在血液中检测到明显的蛋白表达量表达下降。这些结果不仅证明了enUn1Cas12f1在细胞模型中的适用性,也展示了其在动物模型中具备良好的应用潜力,为未来走向基因治疗等临床场景提供了有力支撑。
3. 意料之外的发现:靶向链编辑
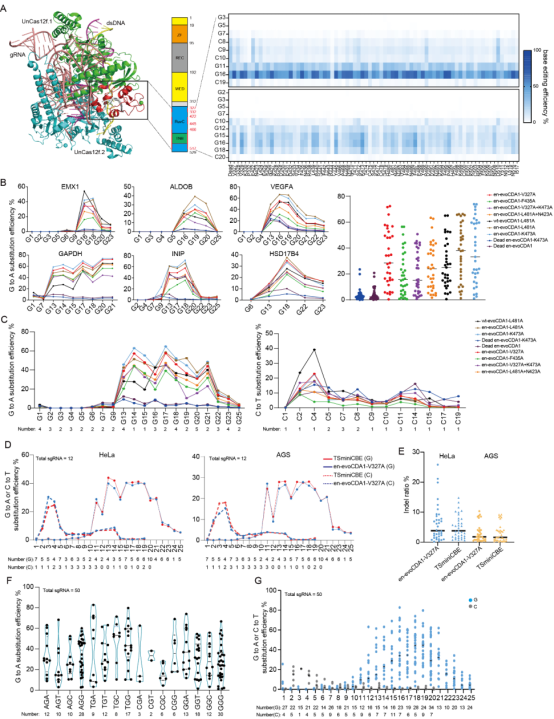
在测试过程中,联合团队观察到一个奇特的现象:基于 enUn1Cas12f1 构建的碱基编辑器不仅能像常规编辑工具一样在DNA的非靶向链上工作,还首次展现出在靶向链上实现C→T高效编辑的能力。这一发现打破了以往对碱基编辑工具的认知。在以往的碱基编辑工具开发工作中,几乎所有优化策略都着眼于非靶向链,靶向链从未进入研究人员的视野。而这一成果首次证明,靶向链同样可以成为有效的编辑对象,极大拓展了碱基编辑的适用范围。
为进一步提高靶向链编辑的效率和纯度,联合团队在evoCDA1-enUn1Cas12f1的基础上通过丙氨酸扫描突变构建了一个高效的靶向链碱基编辑工具,命名为 TSminiCBE。与原始版本相比,TSminiCBE在靶向链上的编辑效率与纯度显著提升。随后,联合团队又引入了一段非特异性DNA结合结构域(HMG-D蛋白),增强编辑器与靶DNA的稳定结合,从而获得性能更优的 HMG-TSminiCBE。在多种人类细胞类型中,HMG-TSminiCBE都表现出稳定且高效的靶向链编辑性能。
4. 推动精准医疗和农业应用
联合团队不仅在细胞水平验证了工具的可行性,还在动物模型中进行了系统性评估。结果显示,改造后的 enUn1Cas12f1 能够通过AAV高效递送至小鼠肝脏,并在 Ttr基因上实现高效编辑(60%),导致血液中目标蛋白水平显著下降,表明enUn1Cas12f1在体内环境下具备良好的编辑活性。
与此同时,联合团队还利用 HMG-TSminiCBE 在 FASN基因上开展了功能验证实验。FASN编码脂肪酸合成酶,是细胞能量代谢和脂质合成中的关键因子,与肥胖、代谢综合征及多种代谢性疾病密切相关。研究发现HMG-TSminiCBE能够在该基因上实现高效的靶向链碱基编辑,并成功引入终止密码子突变(27%),从而为建立代谢性疾病模型提供了新工具。该研究不仅解决了Un1Cas12f1系统编辑效率低下的问题,还首次实现了靶向链碱基编辑,为精准医学、动植物育种等领域提供了全新的工具。

该研究由在线炸金花 、南京师范大学、南京大学、浙江大学、上海科技大学、新疆畜牧科炸金花在线玩 等多家单位合作完成。在线炸金花 王小龙教授、南京师范大学吴丽娜教授和南京大学刘江怀教授为共同通讯作者,在线炸金花 博士生宋梓虢、樊占青、黄舒泓,上海科技大学博士生郭俊璠为论文共同第一作者。我校羊遗传改良与生物育种团队负责人陈玉林教授、浙江大学医炸金花在线玩 黄行许教授、新疆畜牧科炸金花在线玩 郑文新研究员对本研究提供了指导。我校海南研究院和高性能计算平台对本研究提供了大力支持。该研究得到了国家重点研发计划、科技创新2030项目、国家绒毛用羊产业技术体系、江苏省合成生物学中心、陕西省两链融合重大专项、旱区农业陕西重点实验室、陕西省重点领域创新团队等项目支持。
文章链接://www.nature.com/articles/s41467-025-64562-0
